光气()在塑料、制革、制药等工业中有许多用途,工业上采用高温下与在活性炭催化下合成。
(1)实验室常用来制备氯气的化学方程式为
(2)工业上利用天然气(主要成分为)与进行高温重整制备,已知、、和的燃烧热()分别为-890.3、-285.8和-283.0,则生成1(标准状况)所需热量为
(3)实验室中可用氯仿()与双氧水直接反应制备光气,其反应的化学方程式为
(4)的分解反应为。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10到14的浓度变化曲线未示出):
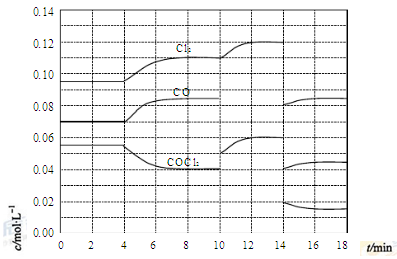
①计算反应在第8时的平衡常数=
②比较第2反应温度(2)与第8反应温度(8)的高低:(2)
(填"<"、">"或"="),
③若12时反应于温度(8)下重新达到平衡,则此时=
④比较产物在2-3、5-6和12-13时平均反应速率(平均反应速率分别以v(2-3)、v(5-6)、v(12-13))的大小
⑤比较反应物在5-6和15-16时平均反应速率的大小:v(5-6)
 N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。


 ;
; 。
。


 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
 2H2↑+O2↑
2H2↑+O2↑ 2H2+O2
2H2+O2 2H2↑+O2↑
2H2↑+O2↑
 粤公网安备 44130202000953号
粤公网安备 44130202000953号