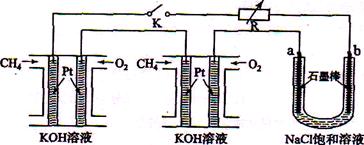
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入和,电解质为溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为、。
(2)闭合开关后,、电极上均有气体产生.其中电极上得到的是,电解氯化钠溶液的总反应方程式为;
(3)若每个电池甲烷通入量为1 (标准状况),且反应完全,则理论上通过电解池的电量为(法拉第常数=9.65×l04.,列式计算),最多能产生的氯气体积为(标准状况)。
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入和,电解质为溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为、。
(2)闭合开关后,、电极上均有气体产生.其中电极上得到的是,电解氯化钠溶液的总反应方程式为;
(3)若每个电池甲烷通入量为1 (标准状况),且反应完全,则理论上通过电解池的电量为(法拉第常数=9.65×l04.,列式计算),最多能产生的氯气体积为(标准状况)。