(7分)实验室制取气体的装置如图所示,根据所学的知识回答下列问题。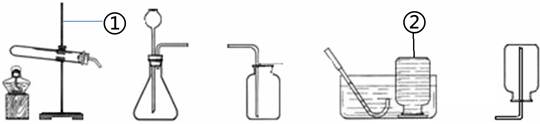
A B C D E
(1)图中标有①、②的仪器名称:① ;② 。
(2)写出用A或B制取氧气的一个化学方程式 ,可选用图中 和 (填标号)组装一套制取较纯氧气的装置,判断氧气集满的方法是 。
(7分)实验室制取气体的装置如图所示,根据所学的知识回答下列问题。
A B C D E
(1)图中标有①、②的仪器名称:① ;② 。
(2)写出用A或B制取氧气的一个化学方程式 ,可选用图中 和 (填标号)组装一套制取较纯氧气的装置,判断氧气集满的方法是 。