利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。当电池工作时,有关说法正确的是( )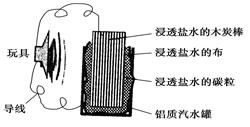
| A.铝罐将逐渐被腐蚀 |
| B.碳粒和炭棒上发生的反应为:O2+4e-=2O2- |
| C.炭棒应与玩具电机的负极相连 |
| D.该电池工作一段时间后炭棒和碳粒的质量会减轻 |
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。当电池工作时,有关说法正确的是( )
| A.铝罐将逐渐被腐蚀 |
| B.碳粒和炭棒上发生的反应为:O2+4e-=2O2- |
| C.炭棒应与玩具电机的负极相连 |
| D.该电池工作一段时间后炭棒和碳粒的质量会减轻 |