下列说法正确的是( )
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH =" —40.69" kJ·mol-1 H2O(l) 的 ΔH =" —40.69" kJ·mol-1 |
| B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍 |
| C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH代表燃烧热 |
| D.已知: |
| 共价键 |
C-C |
C=C |
C-H |
H-H |
| 键能/ kJ·mol-1 |
348 |
610 |
413 |
436 |
则可以计算出反应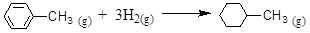 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1
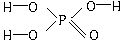 )中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是()
)中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是()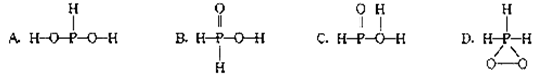

 粤公网安备 44130202000953号
粤公网安备 44130202000953号