小琴同学设计如右图所示的A、B两个实验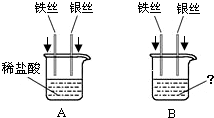
(1)实验时,她为了除去铁丝和银丝表面的氧化物或污物,其操作是 ;
(2)A实验目的是 ,实验时,将铁丝和银丝同时插入稀硫酸中,可观察到的现象是铁丝表面有气泡产生,银丝表面无明显现象,溶液由无色逐渐变为浅绿色;所发生反应的化学方程式为 ;
(3)B实验中,当烧杯内盛有 溶液时,可验证Fe、Ag三种金属活动性强弱。
小琴同学设计如右图所示的A、B两个实验
(1)实验时,她为了除去铁丝和银丝表面的氧化物或污物,其操作是 ;
(2)A实验目的是 ,实验时,将铁丝和银丝同时插入稀硫酸中,可观察到的现象是铁丝表面有气泡产生,银丝表面无明显现象,溶液由无色逐渐变为浅绿色;所发生反应的化学方程式为 ;
(3)B实验中,当烧杯内盛有 溶液时,可验证Fe、Ag三种金属活动性强弱。