如图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。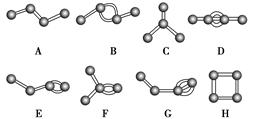
(1)图中属于烷烃的是________(填字母)。
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成________和________;不仅可以形成________,还可以形成碳环。
(3)上图中互为同分异构体的是:A与_____________________。B与________;D与________(填字母)。
如图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
(1)图中属于烷烃的是________(填字母)。
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成________和________;不仅可以形成________,还可以形成碳环。
(3)上图中互为同分异构体的是:A与_____________________。B与________;D与________(填字母)。