维生素C的结构简式如图所示。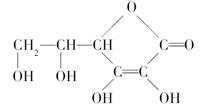
(1)维生素C的分子式是________。
(2)维生素C________溶于水(填“易”或“难”)。
(3)在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有________性。
(4)在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到溶液蓝色退去,说明维生素C具有________性。
(5)中学生每天需补充约60 mg维生素C,下列物质中含有丰富维生素C的是________。
| A.辣椒 | B.鸡蛋 | C.米饭 | D.青霉素 |
维生素C的结构简式如图所示。
(1)维生素C的分子式是________。
(2)维生素C________溶于水(填“易”或“难”)。
(3)在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有________性。
(4)在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到溶液蓝色退去,说明维生素C具有________性。
(5)中学生每天需补充约60 mg维生素C,下列物质中含有丰富维生素C的是________。
| A.辣椒 | B.鸡蛋 | C.米饭 | D.青霉素 |