如图,有甲、乙两容器,甲保持恒压,乙保持恒容,分别向其中充入1 mol A、3 mol B发生可逆反应:A(g)+3B(g)  2C(g)+D(s),下列说法正确的是( )
2C(g)+D(s),下列说法正确的是( )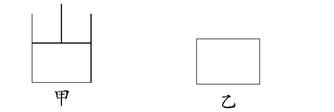
A.当乙中混合气体总质量不再变化时即达到化学平衡
B.达平衡时用A表示反应速率时,v(甲)<v(乙)
C.由于容器甲的容积在不断变化,故从反应开始到平衡所需时间比容器乙要长
D.达到平衡时,甲所需时间短,但两容器中A的转化率相等
如图,有甲、乙两容器,甲保持恒压,乙保持恒容,分别向其中充入1 mol A、3 mol B发生可逆反应:A(g)+3B(g)  2C(g)+D(s),下列说法正确的是( )
2C(g)+D(s),下列说法正确的是( )
A.当乙中混合气体总质量不再变化时即达到化学平衡
B.达平衡时用A表示反应速率时,v(甲)<v(乙)
C.由于容器甲的容积在不断变化,故从反应开始到平衡所需时间比容器乙要长
D.达到平衡时,甲所需时间短,但两容器中A的转化率相等