(14分)请回答下列问题:
(1)下表列出了一些化学键的键能E:
化学键
|
H—H
|
O===O
|
O—H
|
E/kJ·mol-1
|
436
|
x
|
463
|
反应H2(g)+ O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则x=__________。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则x=__________。
(2)铅蓄电池是正极板上覆盖有PbO2,负极板上覆盖有Pb,电解质溶液是H2SO4溶液,电池放电时的总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
请写出充电时阴极的电极反应式:__________________
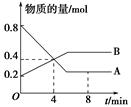
(3)反应m A+n B p C,在某温度下达到平衡。
p C,在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是________________。
②若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向________________方向移动。
③若再升高温度,平衡向逆向移动,则正反应为 _________ 反应(填“吸热”或“放热”)
(4)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。

①请在图中标出电极材料及电解质溶液(写化学式)________________
②盐桥中的Cl-向________极移动(填“左”或“右”)。
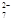 + ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑+ ________
+ ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑+ ________
 K2CO3+6H2O
K2CO3+6H2O
 CH3OH(g) △H="—90.8" kJ·mol—1。
CH3OH(g) △H="—90.8" kJ·mol—1。 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则x=__________。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则x=__________。 p C,在某温度下达到平衡。
p C,在某温度下达到平衡。
 2SO3(g),反应过程的能量变化如图所示。
2SO3(g),反应过程的能量变化如图所示。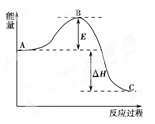
 2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。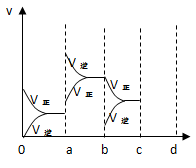
 粤公网安备 44130202000953号
粤公网安备 44130202000953号