常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是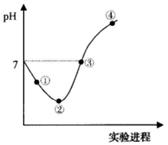
| A.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO﹣ |
| B.③点所示溶液中:c(Na+)= c(HClO)+2c(ClO-) |
| C.实验进程中溶液的pH可以用pH试纸测得 |
| D.曲线的起始点水的电离程度最大 |
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是
| A.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO﹣ |
| B.③点所示溶液中:c(Na+)= c(HClO)+2c(ClO-) |
| C.实验进程中溶液的pH可以用pH试纸测得 |
| D.曲线的起始点水的电离程度最大 |