碳酸钾 (K2CO3) 和硝酸钾 (KNO3) 在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ |
20 |
30 |
50 |
60 |
80 |
|
| 溶解度g/100g水 |
K2CO3 |
110 |
114 |
121 |
126 |
139 |
| KNO3 |
31.6 |
45.8 |
85.5 |
110 |
169 |
(1)30℃时K2CO3的溶解度为 g/100g水。
(2)图1中能表示KNO3溶解曲线的是 (填“甲”或“乙”)。
(3)曲线上M点的含义是 。
(4)要配制100g 10%的KNO3溶液,需要KNO3固体 g。溶液配制过程中,除用到玻璃棒、胶头滴管外,还需用到下 列仪器中的 。(填字母编号)
A.电子天平 B.烧杯 C.漏斗 D.量筒
(5)60℃时500g饱和KNO3溶液蒸发10g水后,再降温到60℃,可析出KNO3晶体 g。
(6)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示。下列有关说法中,正确的有 。(填字母编号)
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数
一定减小

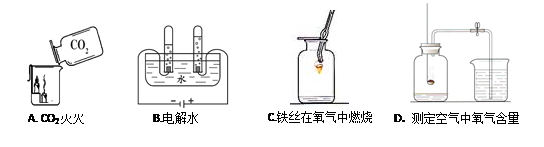
 A实验中观察到的现象是。
A实验中观察到的现象是。 3X+5CO2+19H2O,则X的化学式为。
3X+5CO2+19H2O,则X的化学式为。





 粤公网安备 44130202000953号
粤公网安备 44130202000953号