已知某温度下,在2L密闭容器中加入一定量A,发生以下化学反应:2A(g) 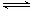 B(g) + C(g);ΔH = −48.25 kJ/L
B(g) + C(g);ΔH = −48.25 kJ/L
时间t与A 、B的浓度有下图所示关系,若测得第15min时c(B)=1.6 mol/L,则下列结论正确的是( )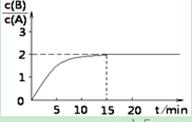
A.该温度下此反应平衡常数为3.2
B.A的初始物质的量为4 mol
C.0-15min内,气体密度不变
D.要使c(B)/c(A)= 3,只能降低反应温度
已知某温度下,在2L密闭容器中加入一定量A,发生以下化学反应:2A(g) 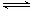 B(g) + C(g);ΔH = −48.25 kJ/L
B(g) + C(g);ΔH = −48.25 kJ/L
时间t与A 、B的浓度有下图所示关系,若测得第15min时c(B)=1.6 mol/L,则下列结论正确的是( )
A.该温度下此反应平衡常数为3.2
B.A的初始物质的量为4 mol
C.0-15min内,气体密度不变
D.要使c(B)/c(A)= 3,只能降低反应温度