下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)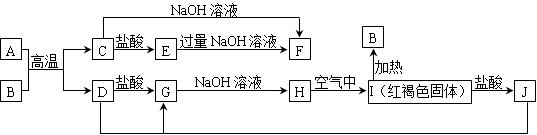
请回答以下问题:
(1)B是_____________,H是_____________(填化学式)
(2)写出J与D反应转化为G的离子方程式_______________________________________
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的离子方程式 _____________
下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)
请回答以下问题:
(1)B是_____________,H是_____________(填化学式)
(2)写出J与D反应转化为G的离子方程式_______________________________________
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的离子方程式 _____________