下图是各物质的反应关系图:已知A和E都是黄色粉末。F有刺激性气味且有漂白性常被不法商人用来漂白腐竹等。请据此回答下列问题: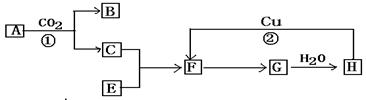
(1)写出下列各物质的化学式:A.__________ H.___________;
(2)写出反应①和反应②的化学方程式:
①___________________________________________________;
②__________________________________________________。
下图是各物质的反应关系图:已知A和E都是黄色粉末。F有刺激性气味且有漂白性常被不法商人用来漂白腐竹等。请据此回答下列问题:
(1)写出下列各物质的化学式:A.__________ H.___________;
(2)写出反应①和反应②的化学方程式:
①___________________________________________________;
②__________________________________________________。