在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示: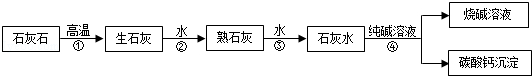
(1)在①﹣④四个过程中,发生了分解反应的是(填序号).
(2)检验烧碱溶液中含有少量
的具体方法是.
(3)在室温下,将53g质量分数为10%的
溶液与3000g澄清石灰水充分混合,恰好完全反应.则这时所得
溶液的质量是多少?(计算结果精确至0.1g)
在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示:
(1)在①﹣④四个过程中,发生了分解反应的是(填序号).
(2)检验烧碱溶液中含有少量
的具体方法是.
(3)在室温下,将53g质量分数为10%的
溶液与3000g澄清石灰水充分混合,恰好完全反应.则这时所得
溶液的质量是多少?(计算结果精确至0.1g)