甲、乙、丙、丁四种物质之间具有如右转化关系: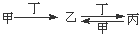 。
。
请回答下列问题:
(1)若乙为两性不溶物,则丙转化为乙的离子方程式为 ;
(2)若丙为形成酸雨的主要物质,则甲的化学式 ,乙能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式为 ;
(3)若丙中含有目前人类使用最广泛的金属元素,且乙转化成丙为化合反应,则将丙溶液蒸发、灼烧得到的物质是 ,除去丙溶液中少量乙的方法是 (用化学方程式表示),如何检验乙溶液中的丙,请设计实验方案 。
甲、乙、丙、丁四种物质之间具有如右转化关系: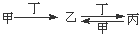 。
。
请回答下列问题:
(1)若乙为两性不溶物,则丙转化为乙的离子方程式为 ;
(2)若丙为形成酸雨的主要物质,则甲的化学式 ,乙能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式为 ;
(3)若丙中含有目前人类使用最广泛的金属元素,且乙转化成丙为化合反应,则将丙溶液蒸发、灼烧得到的物质是 ,除去丙溶液中少量乙的方法是 (用化学方程式表示),如何检验乙溶液中的丙,请设计实验方案 。