下图转化中的字母只代表一种单质或化合物,A是淡黄色固体,B为金属单质,J是白色胶状沉淀,常温下X是液体,C、D、Y均为气体。请回答下列问题: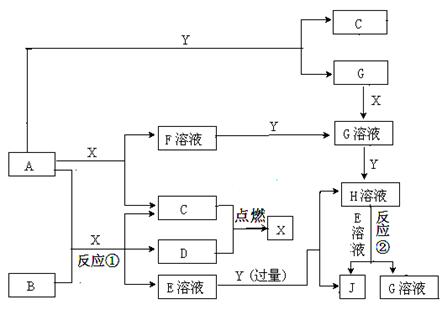
(1)写出化学式: B X
(2)A中存在的化学键类型 H的俗名 Y的电子式
(3)写出下列方程式
反应①的化学方程式
反应②的离子方程式
下图转化中的字母只代表一种单质或化合物,A是淡黄色固体,B为金属单质,J是白色胶状沉淀,常温下X是液体,C、D、Y均为气体。请回答下列问题:
(1)写出化学式: B X
(2)A中存在的化学键类型 H的俗名 Y的电子式
(3)写出下列方程式
反应①的化学方程式
反应②的离子方程式