由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀, 一段时间后某极产生2.24L(标准状况)的气体。问: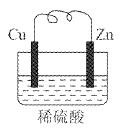
(1)正极是______(填“锌”或“铜”),发生_________反应(填“氧化”或 “还原”)。
(2)负极的电极反应为__________________。
(3)产生这些气体共需转移电子_________mol。
由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀, 一段时间后某极产生2.24L(标准状况)的气体。问:
(1)正极是______(填“锌”或“铜”),发生_________反应(填“氧化”或 “还原”)。
(2)负极的电极反应为__________________。
(3)产生这些气体共需转移电子_________mol。