溴主要以形式存在于海水中,海水呈弱碱性。工业上制备的的操作步骤为:
①一定条件下,将通入浓缩的海水中,生成
②利用热空气将吹出,并用浓溶液吸收,生成、等
③用硫酸酸化步骤②得到的混合物
完成下列填空:
(1)氧化应在条件下进行,目的是为了避免。
(2)可用热空气吹出,其原因是。
(3)写出步骤③所发生的化学反应方程式。
用硫酸而不用盐酸酸化的原因可能是。步骤②的产品有时运输到目的地后再酸化,主要是因为.
(4)为了除去工业Br2中微量的,可向工业中。
a.通入 b.加入溶液 c.加入溶液 d.加入溶液
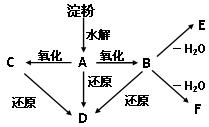
 最难。
最难。 :
: 3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。
3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0.3mol·L-1。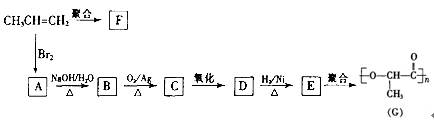
 粤公网安备 44130202000953号
粤公网安备 44130202000953号