研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料。液氨燃烧的化学反应方程式为:4NH3+3O2 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是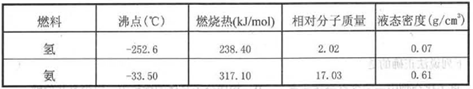
② 以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量少
④氮的液化比氢容易得多
| A.①③ | B.②③ | C.①④ | D.②④ |
研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料。液氨燃烧的化学反应方程式为:4NH3+3O2 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
② 以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量少
④氮的液化比氢容易得多
| A.①③ | B.②③ | C.①④ | D.②④ |