根据下图所示制备气体的装置,回答下列问题(装置选择可用序号填写)。 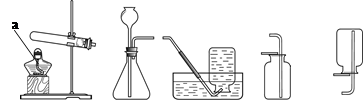
A B C D E
(1)标有字母“a”的仪器名称是 。
(2)用高锰酸钾制取氧气时,有关反应的化学方程式为 ,应选用的装置是 。
(3)用石灰石和稀盐酸制取二氧化碳的化学方程式为 ,所选用的发生装置是 ,收集装置是 ,用燃着的木条检验二氧化碳是否收集满时,可观察到的现象是 。
根据下图所示制备气体的装置,回答下列问题(装置选择可用序号填写)。 
A B C D E
(1)标有字母“a”的仪器名称是 。
(2)用高锰酸钾制取氧气时,有关反应的化学方程式为 ,应选用的装置是 。
(3)用石灰石和稀盐酸制取二氧化碳的化学方程式为 ,所选用的发生装置是 ,收集装置是 ,用燃着的木条检验二氧化碳是否收集满时,可观察到的现象是 。