已知(l) =H2O(g) ΔH1=a kJ·
=H2O(g) ΔH1=a kJ·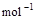
(2)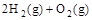 =2H2O(g) ΔH2=b kJ·
=2H2O(g) ΔH2=b kJ·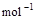
(3) =H2O(l) ΔH3=c kJ·
=H2O(l) ΔH3=c kJ·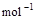
(4)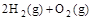 =2H2O(l) ΔH4=d kJ·
=2H2O(l) ΔH4=d kJ·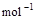
下列关系式中正确的是
| A. a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
已知(l) =H2O(g) ΔH1=a kJ·
=H2O(g) ΔH1=a kJ·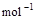
(2)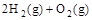 =2H2O(g) ΔH2=b kJ·
=2H2O(g) ΔH2=b kJ·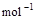
(3) =H2O(l) ΔH3=c kJ·
=H2O(l) ΔH3=c kJ·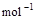
(4)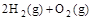 =2H2O(l) ΔH4=d kJ·
=2H2O(l) ΔH4=d kJ·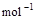
下列关系式中正确的是
| A. a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |