乙炔(C2H2)是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中C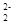 与O
与O 互为等电子体,等电子体结构相似,则1 个O
互为等电子体,等电子体结构相似,则1 个O 中含有的π键数目为 。
中含有的π键数目为 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
。
(3)乙炔与氢氰酸反应可得丙烯腈( H2C=CH—C≡N )。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为________。
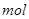 二氧化氯时,转移电子
二氧化氯时,转移电子 粤公网安备 44130202000953号
粤公网安备 44130202000953号