在密闭容器中加入等浓度的CO与H2O,T ℃时发生如下反应:
CO(g)+H2O(g)  CO2(g)+H2(g) ΔH< 0
CO2(g)+H2(g) ΔH< 0
已知CO的浓度变化如图所示,第4 minCO的浓度不再改变。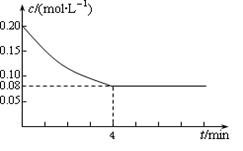
(1)从0~4 min,该反应的平均速率v(CO)= mol/(L·min);该反应的平衡常数表达式为:K= ;可计算得该反应的平衡常数结果为:K= 。
(2)为了增大CO的转化率,可以采取的措施有 。
| A.增大反应物中CO的浓度 |
| B.降低反应温度 |
| C.将密闭容器体积压缩至一半 |
| D.加入适宜的催化剂 |
(3)若不改变反应温度和反应物中CO的起始浓度,使CO的转化率达到90%,则水蒸气的起始浓度至少为 mol/L?
 粤公网安备 44130202000953号
粤公网安备 44130202000953号