小强同学为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。将一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成小球时,撤火,通入氯气,即可见钠着火燃烧。以下叙述错误的是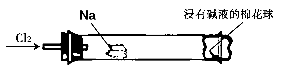
| A.反应生成的大量白色烟雾是氯化钠晶体 |
| B.钠着火燃烧产生苍白色火焰 |
| C.浸有NaOH溶液的棉球用于吸收生成的氯化钠,以免污染空气 |
| D.用湿润的淀粉碘化钾试纸可以检验氯气是否被完全吸收 |
小强同学为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。将一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成小球时,撤火,通入氯气,即可见钠着火燃烧。以下叙述错误的是
| A.反应生成的大量白色烟雾是氯化钠晶体 |
| B.钠着火燃烧产生苍白色火焰 |
| C.浸有NaOH溶液的棉球用于吸收生成的氯化钠,以免污染空气 |
| D.用湿润的淀粉碘化钾试纸可以检验氯气是否被完全吸收 |