下表是元素周期表的一部分,针对表中①~⑩中的元素,回答以下问题:
| ① |
|
|
|||||||||||||||||||||||
| |
|
|
|
② |
③ |
④ |
⑤ |
|
|||||||||||||||||
| ⑥ |
⑦ |
⑧ |
|
|
|
⑨ |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑩ |
|
||||||||
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
| |
|
|
|
|
|
|
|
|
|
(1)在表中a、b、c、d四个区域中,全部是金属元素的区域为 。
(2)在①~⑨元素中,原子半径最大的是 (填元素名称);①和③组成的化合物的电子式为 ;⑨的离子结构示意图为 。
(3)元素的最高价氧化物对应的水化物中酸性最强的是 (填化学式,下同),碱性最强的是 ,呈两性的是 。
(4)⑨和⑩中,非金属性较强的是 (填元素符号);可用一个化学反应说明该事实,写出该反应的离子方程式: 。

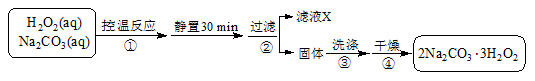
 2Na2CO3·3H2O2(s)ΔH < 0,请回答下列问题:
2Na2CO3·3H2O2(s)ΔH < 0,请回答下列问题: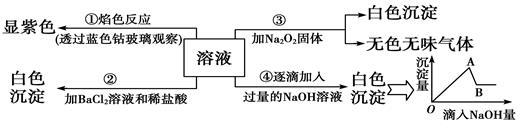
 粤公网安备 44130202000953号
粤公网安备 44130202000953号