某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示。在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗。为使液体顺利流下,还需插入“空气导入管”与大气相通。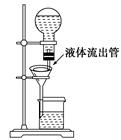
(1)“空气导入管”下口应在________,上口应在________。
| A.滤纸边沿下方 | B.滤纸边沿上方 |
| C.待过滤液液面上 | D.待过滤液中 |
E.A和B项均可 F.C和D项均可
(2)试简要说明自动加液过滤的原理。
某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示。在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗。为使液体顺利流下,还需插入“空气导入管”与大气相通。
(1)“空气导入管”下口应在________,上口应在________。
| A.滤纸边沿下方 | B.滤纸边沿上方 |
| C.待过滤液液面上 | D.待过滤液中 |
E.A和B项均可 F.C和D项均可
(2)试简要说明自动加液过滤的原理。