已知A元素位于元素周期表第三周期,其原子最外层电子数是最内层电子数的一半。甲、乙、丙、丁四种物质均含有A元素,其中乙为白色固体,它们之间的相互转化关系如下图所示,试回答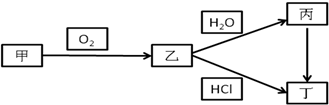
(1)A的元素符号为 ,丁的电子式为
(2)写出乙转化为丙的化学方程式
已知A元素位于元素周期表第三周期,其原子最外层电子数是最内层电子数的一半。甲、乙、丙、丁四种物质均含有A元素,其中乙为白色固体,它们之间的相互转化关系如下图所示,试回答
(1)A的元素符号为 ,丁的电子式为
(2)写出乙转化为丙的化学方程式