为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。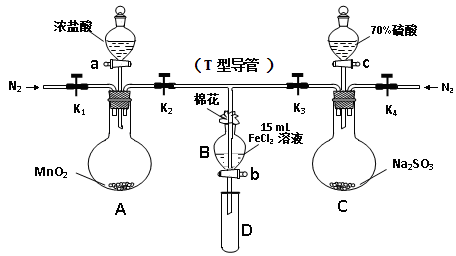
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中, 继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A。
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3。
Ⅵ.更新试管D,重复过程Ⅳ。
(1)过程Ⅰ的目的是 。
(2)棉花中浸润的溶液为 。
(3)A中发生反应的化学方程式为 。
(4)能说明氧化性Fe3+ > SO2的离子方程式是 。
(5)过程Ⅵ,检验B溶液中是否含有SO42-的操作是 。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果不能够证明氧化性Cl2 > Fe3+ > SO2的是 (填“甲”“乙”“丙”),请用必要的文字说明理由 。
| |
过程Ⅳ B溶液中含有的离子 |
过程Ⅵ B溶液中含有的离子 |
| 甲 |
有Fe3+无Fe2+ |
有 Fe2+ |
| 乙 |
既有Fe3+又有Fe2+ |
有SO42- |
| 丙 |
有Fe3+无Fe2+ |
有SO42- |
(7)进行实验过程Ⅴ时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。
查阅资料: Fe2+(aq)+ SO32- (aq)  FeSO3(s)(墨绿色)提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。
FeSO3(s)(墨绿色)提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。
某同学设计如下实验,证实该假设成立:
① 溶液E和F分别为 、 (写化学式)。
②请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因 。
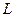 ,再用游标卡尺测量摆球的直径如图所示。
,再用游标卡尺测量摆球的直径如图所示。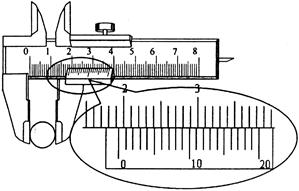
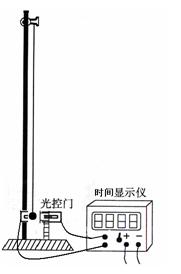
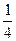 摆长,闭合时间显示仪开关,由静止释放摆球,从时间显示仪读出摆球挡光时间
摆长,闭合时间显示仪开关,由静止释放摆球,从时间显示仪读出摆球挡光时间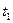 。
。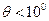 ),由静止释放摆球,用秒表测出摆球作N次全振动的时间是
),由静止释放摆球,用秒表测出摆球作N次全振动的时间是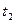
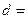 cm
cm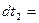 (用字母表示各物理量),就验证了摆球运动过程中机械能守恒。
(用字母表示各物理量),就验证了摆球运动过程中机械能守恒。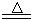 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
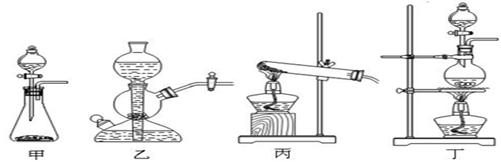
 步骤)
步骤)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号