下图为一个金属铜的晶胞,请完成以下各题。
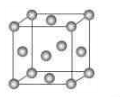
1)该晶胞“实际”拥有的铜原子数是 个。
2)该晶胞称为 。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
3)此晶胞立方体的边长为a cm,Cu的相对原子质量为64。阿伏加德罗常数为NA 。金属铜的晶体密度ρ为 g/cm3。(用a、NA 表示)。
4)铜原子采取的这种堆积方式的空间利用率为 。(填数值)
下图为一个金属铜的晶胞,请完成以下各题。

1)该晶胞“实际”拥有的铜原子数是 个。
2)该晶胞称为 。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
3)此晶胞立方体的边长为a cm,Cu的相对原子质量为64。阿伏加德罗常数为NA 。金属铜的晶体密度ρ为 g/cm3。(用a、NA 表示)。
4)铜原子采取的这种堆积方式的空间利用率为 。(填数值)