将W g木炭与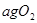 同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为
同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为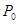 ,高温下容器中木炭与
,高温下容器中木炭与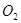 均完全反应后恢复到原温度,压力表的示数为
均完全反应后恢复到原温度,压力表的示数为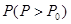 ,试求:
,试求:
(1)当W取值发生变化时,反应后压强P也发生变化,P的最大值(以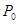 表示)是______。
表示)是______。
(2)以W表示满足题设条件的a的取值范围__________。
(3)在题设条件下,W、a、P、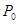 之间必须满足函数系W=f(a、
之间必须满足函数系W=f(a、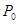 、P),写出该函数表达式:__________________。
、P),写出该函数表达式:__________________。
将W g木炭与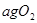 同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为
同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为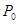 ,高温下容器中木炭与
,高温下容器中木炭与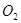 均完全反应后恢复到原温度,压力表的示数为
均完全反应后恢复到原温度,压力表的示数为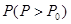 ,试求:
,试求:
(1)当W取值发生变化时,反应后压强P也发生变化,P的最大值(以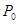 表示)是______。
表示)是______。
(2)以W表示满足题设条件的a的取值范围__________。
(3)在题设条件下,W、a、P、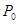 之间必须满足函数系W=f(a、
之间必须满足函数系W=f(a、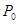 、P),写出该函数表达式:__________________。
、P),写出该函数表达式:__________________。