某实验小组利用废硫酸液制备K2SO4的流程如下:
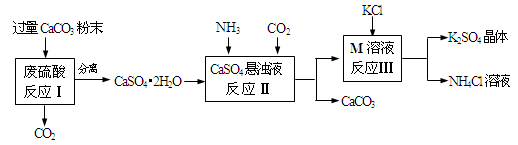
⑴ 将CaCO3研成粉末的目的是。
⑵ 上述流程中可循环使用的物质有CO2和(填写化学式)。
⑶反应Ⅲ中相关物质的溶解度如下表所示。你认为反应Ⅲ在常温下能实现的原因是
。
物质
|
KCl
|
K2SO4
|
NH4Cl
|
M
|
溶解度/g(25℃)
|
34.0
|
11.1
|
37.2
|
19.5
|
⑷ 为了得到较纯的K2SO4晶体,常用饱和K2SO4溶液洗涤反应Ⅲ所得晶体。为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入(选填序号,下同),振荡、静置,再向上层清液中滴加,观察现象即可判断。
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液