分子式为C2H4O2的结构可能有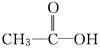 和
和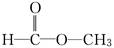 两种,为对其结构进行物理方法鉴定,可用__________________或______________________.
两种,为对其结构进行物理方法鉴定,可用__________________或______________________.
(1)若为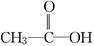 ,则红外光谱中应该有________个振动吸收;核磁共振氢谱中应该有________个峰.
,则红外光谱中应该有________个振动吸收;核磁共振氢谱中应该有________个峰.
(2)若为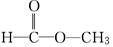 ,则红外光谱中有________个振动吸收;核磁共振氢谱中应有________个峰.
,则红外光谱中有________个振动吸收;核磁共振氢谱中应有________个峰.
分子式为C2H4O2的结构可能有 和
和 两种,为对其结构进行物理方法鉴定,可用__________________或______________________.
两种,为对其结构进行物理方法鉴定,可用__________________或______________________.
(1)若为 ,则红外光谱中应该有________个振动吸收;核磁共振氢谱中应该有________个峰.
,则红外光谱中应该有________个振动吸收;核磁共振氢谱中应该有________个峰.
(2)若为 ,则红外光谱中有________个振动吸收;核磁共振氢谱中应有________个峰.
,则红外光谱中有________个振动吸收;核磁共振氢谱中应有________个峰.