在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)
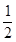 N2(g)+CO2(g) ΔH="-373.2" kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g) ΔH="-373.2" kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)
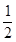 N2(g)+CO2(g) ΔH="-373.2" kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g) ΔH="-373.2" kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |