根据物质相似性、特殊性来学习元素性质是常见的学习方法。
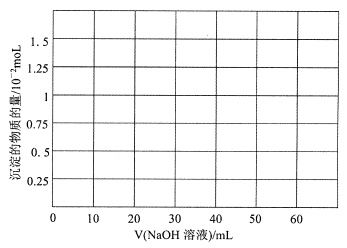
(1)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式_____,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2 BeO2+2H2 O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加人量的变化图:
(2)锗与硅元素相似,锗也是良好的半导体,以下是工业冶炼锗的简单流程图:

①GeCl4的晶体类型为__________。
②写出过程III发生反应的化学方程式__________。
③以下有关工业冶炼锗的说法正确的是__________。
| A.GeO2与SiO2性质相似,均易与盐酸反应 |
| B.过程II的蒸馏是利用GeCl4难溶于水的性质实现的 |
| C.过程IV发生的反应中,GeO2作氧化剂 |
| D.上述过程涉及的基本反应类型有复分解反应、置换反应 |
(3)某同学为了探究硫与浓硝酸的反应产物,将硫与浓硝酸混合,结果生成一种纯净无色气体A,A遇空气变红棕色,据此写出硫与浓硝酸反应的化学方程式___________________。