我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示。请解答下列问题: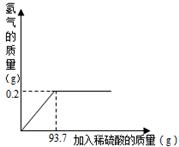
(1)完全反应后,生成H2的质量为 。
(2)该黄铜样品中铜的质量分数为多少?(写出计算过程)
我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分数,取10g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示。请解答下列问题:
(1)完全反应后,生成H2的质量为 。
(2)该黄铜样品中铜的质量分数为多少?(写出计算过程)