已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最多的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E原子的核外电子排布式为 ,A、B、C、D的第一电离能最小的是
(2)B的氧化物的熔点远高于D的氧化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子是 杂化,D的低价氧化物的空间构型为
(4)A、C形成某种化合物的晶胞结构如右图所示,则其化学式为 
(5)E单质的晶体的晶胞结构如下图。若E原子的半径是r cm,则E单质的密度的计算公式是 (用NA表示阿伏伽德罗常数)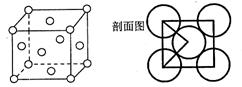

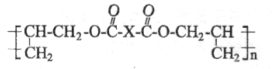 X为未知部分的结构,各物质间有如下转化:
X为未知部分的结构,各物质间有如下转化:

 ,分子内所有碳原子共平面,D在一定条件下可以生成五元环酯,其结构简式是______________。
,分子内所有碳原子共平面,D在一定条件下可以生成五元环酯,其结构简式是______________。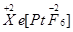 、
、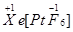 两种可能,经证实
两种可能,经证实 不溶于
不溶于 等非极性溶剂。”据此可确定
等非极性溶剂。”据此可确定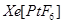 中化学键类型为________。
中化学键类型为________。 采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是________,
采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是________,
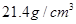 则Pt原子的半径为_________pm(Pt的相对原子质量195.1)
则Pt原子的半径为_________pm(Pt的相对原子质量195.1) 和
和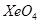 ,它们都有很强的氧化性,
,它们都有很强的氧化性,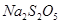 )常用作食品漂白剂,其制备工艺流程如下:
)常用作食品漂白剂,其制备工艺流程如下: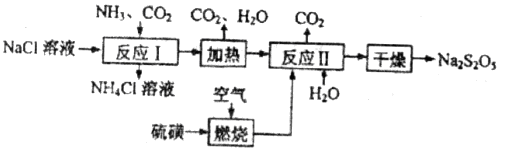
 等多步反应。
等多步反应。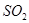 ,其离子方程式为___________。
,其离子方程式为___________。 溶液喷淋“捕捉”空气中的
溶液喷淋“捕捉”空气中的 。
。 为原料可合成化肥尿素[
为原料可合成化肥尿素[ ]。已知:
]。已知:
 ①
①
 ②
②
 ③
③ ,在催化剂作用下CO和
,在催化剂作用下CO和 反应生成甲醇:
反应生成甲醇: 某容积可变的密闭容器中充有10molCO与20mol
某容积可变的密闭容器中充有10molCO与20mol
 _______VL。(填“大于”、“小于”或“等于”)
_______VL。(填“大于”、“小于”或“等于”) _______
_______ (填“>”、“<”或“=”)
(填“>”、“<”或“=”) 粤公网安备 44130202000953号
粤公网安备 44130202000953号