二甲醚(
)是无色气体,可作为一种新型能源。由合成气(组成为
、
和少量的
)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:
(i)
+ 2
=
= -90.1
•
(ii)
+ 3
=
+
= -49.0
•
水煤气变换反应:
(iii)
+
=
+
= -41.1
•
二甲醚合成反应:
(iV)2
=
+
= -24.5
•
回答下列问题:
(1)
是合成气直接制备二甲醚反应催化剂的主要成分之一。工业上从铝土矿制备较高纯度
的主要工艺流程是(以化学方程式表示)。
(2)分析二甲醚合成反应(iV)对于
转化率的影响。
(3)由
和
直接制备二甲醚(另一产物为水蒸气)的热化学方程式为。根据化学反应原理,分析增加压强对直接制备二甲醚反应的影响。
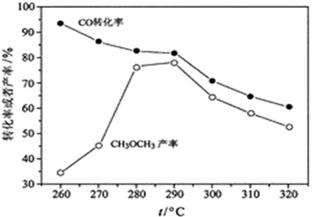
(4)有研究者在催化剂(含
-
-
-
和
)、压强为5.0
的条件下,由
和
直接制备二甲醚,结果如下图所示。其中
转化率随温度升高而降低的原因是。
(5)二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度等于甲醇直接燃料电池(5.93
•
•
)。若电解质为酸性,二甲醚直接燃料电池的负极反应为,一个二甲醚分子经过电化学氧化,可以产生个电子的能量;该电池的理论输出电压为1.20
,能量密度
=(列式计算。能量密度=电池输出电能/燃料质量,1
•
= 3.6×106
)。