某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
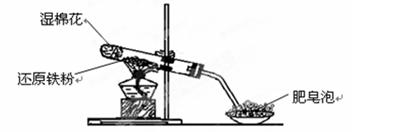
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许固体物质于试管中,并向试管中加稀硫酸得溶液B;
②取少量溶液B于试管中,滴加几滴KSCN溶液,结果溶液未变红色,说明硬质试管中固体物质的成分有:__________________。(填化学式)
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,
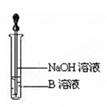
可观察到先生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请按顺序写出与上述现象相关的反应方程式:属于离子反应的只写离子方程式。①②
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明Fe2+ 具有性。由此可知,实验室中FeSO4溶液在保存时要加入少量铁粉,其原因是_________________。(用离子方程式表示)