在下列图象中,横坐标表示加入试剂的体积V,纵坐标表示沉淀的质量m。根据实验内容把相对应曲线标号填入横线上。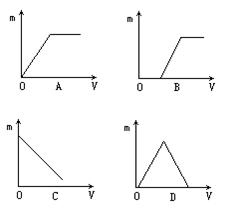
(1)在澄清石灰水中通入CO2,直至过量。
(2)在硫酸和盐酸混合溶液中滴加氢氧化钡溶液,直至过量。
(3)在碳酸钡的悬浊液中加盐酸,直至过量。
回答:(1)_______(2)________(3)________。
在下列图象中,横坐标表示加入试剂的体积V,纵坐标表示沉淀的质量m。根据实验内容把相对应曲线标号填入横线上。
(1)在澄清石灰水中通入CO2,直至过量。
(2)在硫酸和盐酸混合溶液中滴加氢氧化钡溶液,直至过量。
(3)在碳酸钡的悬浊液中加盐酸,直至过量。
回答:(1)_______(2)________(3)________。