(12分)已知25℃时部分弱电解质的电离平衡常数数据如下表:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
| 平衡常数 |
Ka=1.8×10-5 |
Ka1=4.3×10-7 Ka2=5.6×10-11 |
Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的四种溶液:
A、CH3COOH B、Na2CO3 C、NaClO D、NaHCO3;
pH由小到大的排列顺序是 ;adcb(用字母表示)
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是( )
A、c(H+) B、c(H+)/c(CH3COOH)
C、c(H+)•c(OH-) D、c(OH-)/c(H+)
E、c(H+)•c( CH3COO-)/(CH3COOH)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 大于CH3COOH的电离平衡常数(填大于、小于或等于),理由是 . 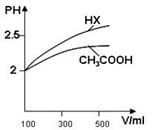
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中
c(CH3COO-)—c(Na+)= (填精确值),c(CH3COO-)/c(CH3COOH)= 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号