有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是
途径① S H2SO4
H2SO4
途径② S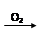 SO2
SO2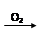 SO3
SO3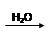 H2SO4
H2SO4
| A.途径①反应中体现了浓HNO3的强氧化性和酸性 |
| B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本 |
| C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- |
| D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高 |
有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是
途径① S H2SO4
H2SO4
途径② S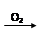 SO2
SO2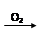 SO3
SO3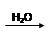 H2SO4
H2SO4
| A.途径①反应中体现了浓HNO3的强氧化性和酸性 |
| B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本 |
| C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- |
| D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高 |