(3分)在一烧杯中盛有21.4g Na2CO3和NaCl组成的固体混合物。向其中逐渐滴加溶质质量分数为10%的稀盐酸。放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中B点时,烧杯中溶液的
pH 7(填 >、=或<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。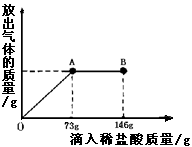
(3分)在一烧杯中盛有21.4g Na2CO3和NaCl组成的固体混合物。向其中逐渐滴加溶质质量分数为10%的稀盐酸。放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中B点时,烧杯中溶液的
pH 7(填 >、=或<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。