小军根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木炭代替红磷测定空气中氧气的含量,并按右图装置进行实验。
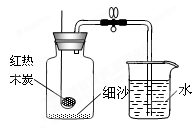
①小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象。请认真分析,小军实验失败的原因是什么?(答一条即可)
②小军将集气瓶中的细沙改为石灰水,重复上述①实验,有倒吸现象,因为石灰水可吸收一部分生成的二氧化碳,但小军还发现倒吸的水量未达到集气瓶内原剩余容积的1/5。原因可能是什么?(答一条)
③小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择和生成物的要求上应满足什么条件(各答一条)。