钢铁是人类生活和生产中非常重要的材料,但全世界每年都有约四分之一的钢铁因生锈损失。某化学课外小组对钢铁制品锈蚀的条件进行了如下探究,设计了如图所示的实验,据此完成下列有关问题: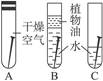
(1)一周后观察到编号为___________________的试管中的铁钉锈蚀严重。
(2)常温下,铁锈蚀是铁跟______________和______________等物质相互作用的结果。
钢铁是人类生活和生产中非常重要的材料,但全世界每年都有约四分之一的钢铁因生锈损失。某化学课外小组对钢铁制品锈蚀的条件进行了如下探究,设计了如图所示的实验,据此完成下列有关问题:
(1)一周后观察到编号为___________________的试管中的铁钉锈蚀严重。
(2)常温下,铁锈蚀是铁跟______________和______________等物质相互作用的结果。