磷是存在于自然界和生物体内的的重要元素。回答下列与磷及其化合物有关的问题。
(1)磷在自然界里主要以 的形式存在于矿石中,这些磷矿石 溶于水,其中的磷元素 被作物吸收。
(2)磷(相对原子质量为31)在空气中燃烧生成的氧化物通常可用做强干燥剂。制备100g这种干燥剂所消耗的空气的体积约为 L(在标准状况下)。
(3)有机磷农药“乐果”的结构简式是: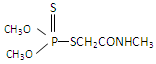 ,其中所含的双键有 个。
,其中所含的双键有 个。
磷是存在于自然界和生物体内的的重要元素。回答下列与磷及其化合物有关的问题。
(1)磷在自然界里主要以 的形式存在于矿石中,这些磷矿石 溶于水,其中的磷元素 被作物吸收。
(2)磷(相对原子质量为31)在空气中燃烧生成的氧化物通常可用做强干燥剂。制备100g这种干燥剂所消耗的空气的体积约为 L(在标准状况下)。
(3)有机磷农药“乐果”的结构简式是: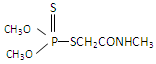 ,其中所含的双键有 个。
,其中所含的双键有 个。