(3分)氨在国民经济中占有重要的地位,请参与下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。
C(s)+H2O(g) H2(g)+CO(g)表 ΔH=+131.3 kJ,ΔS=+133.7 J/K
H2(g)+CO(g)表 ΔH=+131.3 kJ,ΔS=+133.7 J/K
该反应在低温下能否自发反应__________(填“能”或“否”)。
(2)已知在400℃时,N2(g)+3H2(g) 2NH3(g)的K′=0.5。
2NH3(g)的K′=0.5。
①2NH3(g) N2(g)+3H2(g)的K=__________(填数值)。
N2(g)+3H2(g)的K=__________(填数值)。
②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v(N2)正__________v(N2)逆(填“>”、“<”、“=”或“不确定”)。
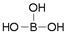 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面 元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。 ,此反应属于________反应(从分解、化合、置换、复分解反应中选择填空)。有人据此认为碘的非金属性比氯强,你认为对吗?(错对与否,都需说明原因)
,此反应属于________反应(从分解、化合、置换、复分解反应中选择填空)。有人据此认为碘的非金属性比氯强,你认为对吗?(错对与否,都需说明原因)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号