常温下电解200mLNaCl、CuSO4的混合溶液,所得气体的体积随时间变化如下图所示,根据图中信息回答下列问题。(气体体积已换算成标准状况下的体积,且忽略气体在水中的溶解和溶液体积的变化)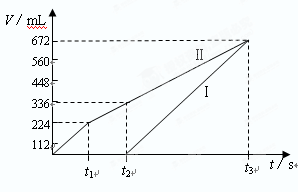
⑴图中曲线________(填Ⅰ或Ⅱ)表示阳极产生气体的变化;
⑵求NaCl和CuSO4的物质的量浓度;
⑶求t2时所得溶液的H+的物质的量浓度。
常温下电解200mLNaCl、CuSO4的混合溶液,所得气体的体积随时间变化如下图所示,根据图中信息回答下列问题。(气体体积已换算成标准状况下的体积,且忽略气体在水中的溶解和溶液体积的变化)
⑴图中曲线________(填Ⅰ或Ⅱ)表示阳极产生气体的变化;
⑵求NaCl和CuSO4的物质的量浓度;
⑶求t2时所得溶液的H+的物质的量浓度。