有关实验操作: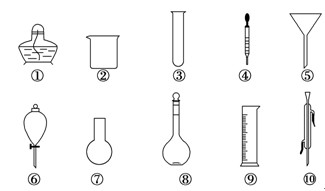
(1)能作反应容器且可直接加热的仪器是上述中的_____________ (填名称)。
(2)仪器上标有温度的是________(填序号)。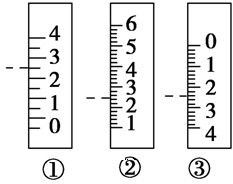
(3)如图是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是________。
| A.①是量筒,读数为2.5 mL | B.③是滴定管,读数为2.5 mL |
| C.②是量筒,读数为2.5 mL | D.②是温度计,读数是2.5 ℃ |
有关实验操作:
(1)能作反应容器且可直接加热的仪器是上述中的_____________ (填名称)。
(2)仪器上标有温度的是________(填序号)。
(3)如图是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是________。
| A.①是量筒,读数为2.5 mL | B.③是滴定管,读数为2.5 mL |
| C.②是量筒,读数为2.5 mL | D.②是温度计,读数是2.5 ℃ |